合作单位:Chinese Academy of Tropical Agricultural Sciences
参考文献:Shanying Zhang, Xiaolei Li, Binling Ai, et al. Food Chemistry: X, 2022. DOI:https://doi.org/10.1016/j.fochx.2022.100369.(IF = 6.4)
背景:
晚期糖基化终产物(AGEs)是食品加工和贮藏过程中美拉德反应产生的一类有害产物。留在体内的AGEs会诱发癌症和慢性疾病。因此,控制食源性AGEs对提高食品安全和预防相关疾病具有重要意义。
膳食酚类物质被证明是食物中AGEs形成的有效抑制剂。然而,酚类物质随贮存时间的延长抑制作用会被削弱,此外,在食品加工过程中,由于热降解和转化,强化的膳食酚类物质的抗氧化能力也会下降。因此,提高食品中酚类物质的热稳定性和光稳定性是十分重要的。槲皮素(QT)、阿魏酸(FA)和香草酸(VA)是存在于许多水果、花卉、蔬菜和草药中的酚类物质,QT、FA和VA均能抑制AGEs的形成。
研究表明,酚类物质与蛋白质的络合作用有助于它们的可持续性和生物利用度。β-乳球蛋白(β-LG)是主要的乳清蛋白之一,含有多个结合位点,因此可以结合不同类型的各种配体。蛋白质与酚类化合物的特异性或非特异性结合提高了酚类化合物的稳定性。尽管酚类化合物的抗糖基化活性已经在化学模型和体外实验中得到了显著的描述,但很少有研究研究β-LG与单一配体结合对热稳定性和光稳定性或β-LG结构的影响。
方案设计:
在本研究中,β-LG被用作FA、QT和VA配体的载体蛋白,这些配体都被认为可以抑制AGEs的形成。采用荧光光谱、等温滴定量热法(ITC)、圆二色法(CD)、傅立叶变换红外光谱(FTIR)等方法研究β-LG与FA/QT/VA的结合机理,采用高效液相色谱法(HPLC)分析FA/QT/VA与β-LG结合后稳定性的变化。经与魔德科技(www.modekeji.cn)技术团队沟通,拟通过分子对接和分子动力学分析模拟β-LG与FA/QT/VA之间的精确结合位点,可视化并进一步了解β-LG与FA/QT/VA之间的相互作用。
主要结果:
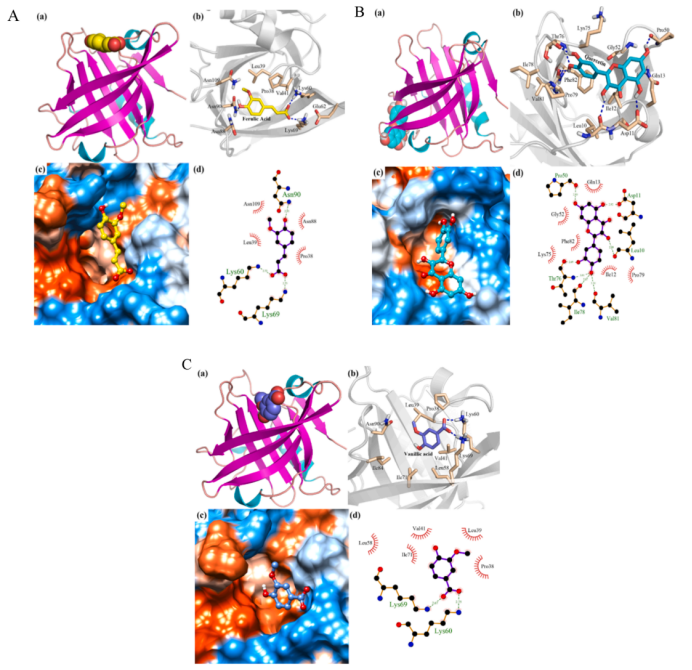
图1 FA (A)、QT (B)、VA(C)和β-LG的结合模型图 (FA/QT/VA与β-LG的三维结合模式(a); VA与周围氨基酸残基之间的相互作用,蓝色虚线表示氢键相互作用(b); VA与β-LG疏水表面的结合,蓝色和橙色部分分别代表β-LG的亲水性和疏水性部分(c); VA与β-LG的二维结合模式,绿色虚线表示氢键相互作用,红色齿轮形表示疏水相互作用(d))
如图1A-C所示,FA结合位点位于β-LG β桶顶部的疏水口袋中。QT结合在β-LG β桶结构的底部口袋,而VA结合在β-LG β桶的顶部。酚类物质与蛋白质的结合涉及多种非共价相互作用,包括氢键、范德华相互作用、π-π堆叠相互作用和疏水相互作用。结合是FA/QT/VA与氨基酸残基相互作用的结果。根据对接结果,与FA和VA相比,QT结构有大量的羟基,与周围的氨基酸残基形成更多的氢键。β-LG分别有3个、6个和5个氨基酸残基与FA/QT/VA疏水相互作用。范德华力是维持酚类化合物和β-LG配合物稳定性的另一个重要的非共价相互作用。QT与Phe82形成π-π堆叠相互作用,增强了QT与β-LG的亲和性。因此,对接分析结果表明,范德华力、疏水相互作用和氢键在酚类物质与β-LG的相互作用中起着重要作用。
酚类物质到蛋白质质心的距离可以用质心距离(DCOM)来表示。FA与β-LG之间的DCOM由1.4 nm减小到接近1.0 nm。这表明FA逐渐延伸到β-L的疏水性口袋中,形成更稳定的FA-β-LG化合物。而在分子动力学模拟过程中,QT与β-LG之间稳定的DCOM,主要归因于QT与周围氨基酸形成氢键的分子结构,具有相对稳定的结合构象。然而,由于VA的分子结构较小,与周围氨基酸残基的非共价相互作用相对较弱,因此在分子动力学模拟过程中,VA与β-LG之间的DCOM并不稳定。
FA、VA和QT对β-LG的结合能分别为79.79±6.45 kJ/mol、−41.65±8.28 kJ/mol和27.77±6.84 kJ/mol。FA与β-LG的结合能最高,VA与β-LG的结合能最低。结合自由能的负值越高,配体越容易与受体结合。QT与VA之间较弱的相互作用能与FA质心距离的波动吻合较好。因此,3种酚类化合物与β-LG的亲和度依次为 FA > QT > VA。
结论:
将能减少AGEs产生的阿魏酸(FA)、槲皮素(QT)和香草酸(VA)包埋于牛β-乳球蛋白(β-LG)中,研究其相互作用机制。荧光实验表明,FA和QT表现为典型的静态猝灭,而VA则引起β-LG的荧光增敏。此外,酚类物质通过诱导β-LG从α-螺旋结构转变为β-结构,改变了β-LG的二级结构,范德华力和氢键是主要动因。FA/ QT/VA与β-LG结合后,其热稳定性和光稳定性显著提高。结果表明,β-LG包埋能有效改善食品中膳食酚类物质的热稳定性和光稳定性。本研究提高了我们对β-LG与酚类物质之间结合相互作用的理解,并可能有助于开发用于食品工业的有效的AGEs抑制剂。